Nat Genet | 超级增强子介导的基因门控影响癌基因MYC表达
超级增强子 (Super enhancer, SE) 是一类具有超强转录激活特性的顺式调控元件,2013年由美国学者Richard A. Young首次提出。近些年来研究发现,超级增强子在癌症发生、细胞分化、免疫应答等重要生物学过程中发挥着重要调控功能,其所调控的基因包含原癌及抑癌基因、细胞身份决定基因、炎症通路关键基因等,具有重要研究价值,已成为生物医学领域一个新的研究热点。2019年11月29日,瑞典卡罗林斯卡大学医院研究人员Rolf Ohlsson、AnitaGöndör等合作在Nature Genetics杂志上发表了题为WNT signaling and AHCTF1 promoteoncogenic MYC expression through super-enhancer-mediated gene gating的文章。他们发现超级增强子可以介导致癌基因MYC与核孔连接,进而促进了MYC转录本从核输出并降低了其降解的效率。

为了构建染色质网络并确定它们与NUP 153的关系,作者用Nodewalk实验和全基因组NUP153免疫沉淀实验分析,确定了染色质网络节点与NUP 153存在的关系,发现MYC基因两侧拓扑域内增强子区被NUP153大量富集(图一)。另外,尽管在MYC启动子上几乎没有或不发生NUP133结合,但NUP133显示了在致癌超级增强子(OSEs)区域内的癌细胞特异性。因此NUP153和NUP133与OSE的结合,表示OSE和MYC在核孔处的分工进行。
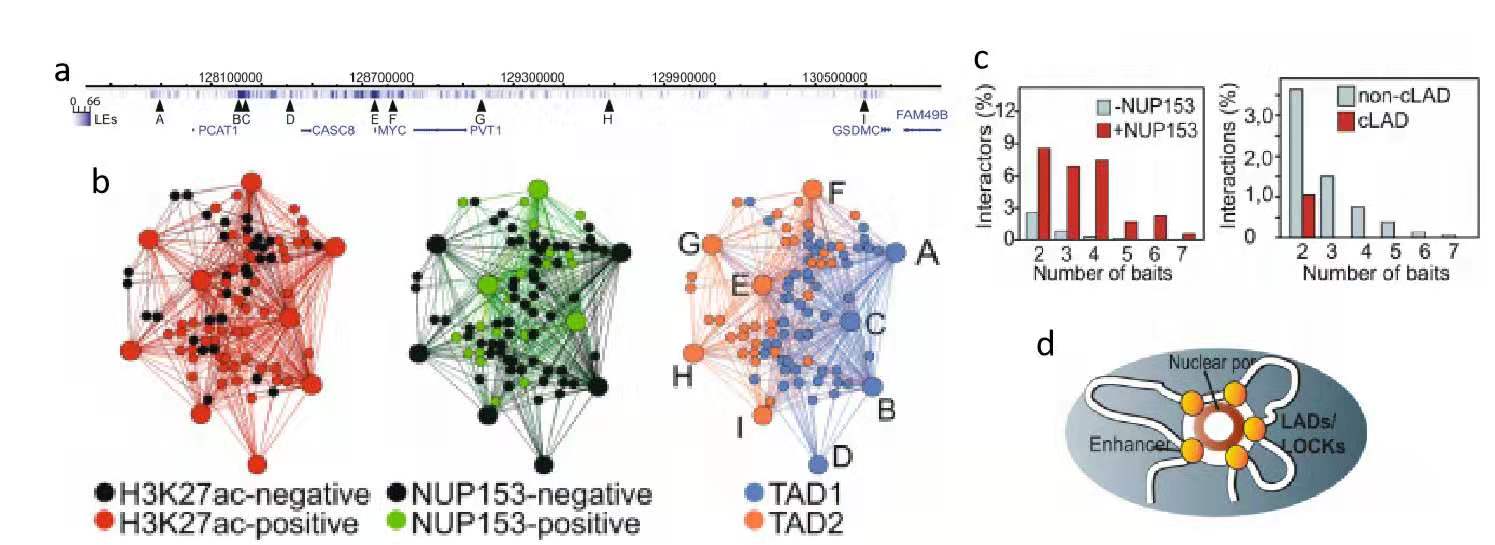
图一:HCT-116细胞染色质网络、增强子和NUP153之间的关系
其次作者结合Nodewalk实验和高通量测序(图二),发现在结肠癌细胞(HCT-116)中核孔蛋白NUP133可能与OSEs结合,并用ChrISP(chromatin in situ proximity,染色质原位邻位连接分析)实验验证了Nup133和OSE相互作用。而为了探究超级增强子是否与基因的转录有关,作者比较了HCT-116细胞中MYC的新生RNA,胞质RNA以及总RNA的表达量和降解情况,发现细胞中MYC 转录本能够被快速的从核内输出从而逃脱了在核内的高降解率。
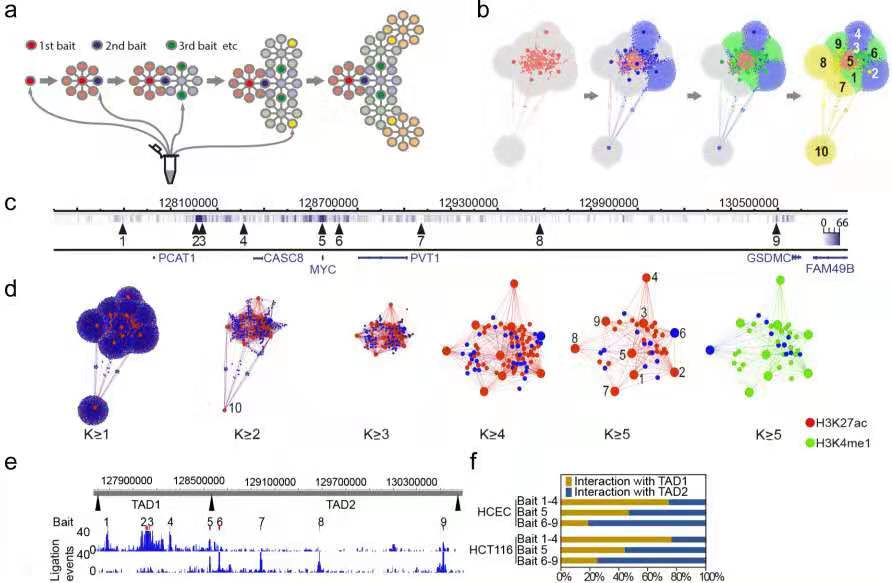
图二:Nodewalk网络及他们与增强子的联系
接下来为了探究这种从核内输出的机制,作者关注了NUP107复合物的中心蛋白AHCTF1。并结合ChIP 和 ChrISP实验分析发现AHCTF1是OSE锚定到核孔所必须的蛋白。在经典的Wnt通路中β-catenin与TCF4复合物起着关键的作用且介导着MYC基因的表达,为了进一步了解AHCTF1,β-catenin和OSE之间的相互作用,作者研究了Wnt通路中MYC增强子的TCF4结合位点。ChIP分析表明,AHCTF1结合到TCF4结合位点区域比结合到MYC启动子区域强。因此,作者认为β-catenin在TCF4结合位点上介导了AHCTF1和核孔蛋白向OSE的募集。β-catenin 通过OSE介导的MYC向核孔转运的基因门控调节了胞质MYC mRNA 转录后的水平。综上所述,在癌细胞中OSE会介导有转录活性的MYC等位基因导入核孔并让其逃脱在核孔内的高降解率。
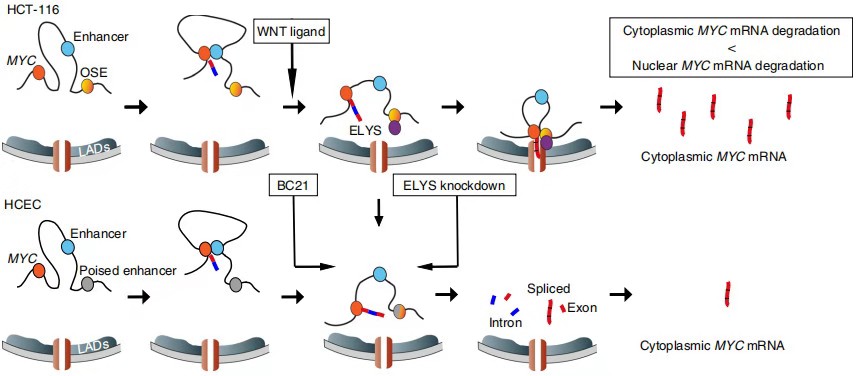
总之,β-catenin通过典型的Wnt信号通路启动OSE介导的基因门控,并在转录后调节MYC 基因的mRNA胞质水平(图三)。因此关于超级增强子介导致癌基因表达及其机制的探索有望给癌症治疗带来希望。
原文:Scholz BA, et al. WNT signaling and AHCTF1 promote oncogenic MYC expression through super-enhancer-mediated gene gating. Nat Genet. 2019 Dec;51(12):1723-1731.
- - - 推荐阅读 - - -

Gut: 复旦大学研究团队发现血浆细胞外囊泡长链RNA谱应用于胰腺导管腺癌的诊断
细胞外囊泡(extracellularvesicle,EV)是一种由活细胞分泌的纳米级别小囊泡,通过运输核酸和蛋白等活性分子来介导细胞间的通讯。细胞外囊泡及其内容物具有组织特异性并且可以反映其母细胞的特征,因而成为疾病
2019-10-23

2019国自然超级增强子、RNA修饰、胞外囊泡项目解析
8月16日,翘首以盼的国家自然科学基金项目终于公布了。在医学与生物学相关研究领域中,表观遗传学现有的研究成果,是咱们华人科学家贡献比较多的一个领域。而从2019年国家自然科学基金中,我们也看到了许多令人兴
2019-08-30

Nature | 相分离调控转录起始至转录延伸的转换过程
本文转载自公众号BioArt 撰文|赤贞 责编|兮 近年来,“相分离”相关研究十分火热,自从TonyAHyman等人发现相分离现象之后,许多团队对相分离在复杂的生物学过程中所起到的重要
2019-08-21
