客户文章 | 南方医院李国新团队揭示mRNA ac4C修饰调控胃癌细胞缺氧耐受新机制
抗血管生成治疗已成为多种实体瘤的一线或二线治疗方案,有效提高肿瘤患者生存预后。然而,肿瘤细胞对缺氧的内在抵抗是限制抗血管生成治疗效果的重要因素,但其潜在机制尚不清楚。
近日,南方医科大学南方医院李国新教授团队在国际权威学术期刊Advanced Science上在线发表题为“N4‐Acetylcytidine Drives Glycolysis Addiction in Gastric Cancer via NAT10/SEPT9/HIF‐1a Positive Feedback Loop”的原创性研究论文,该项成果被精选为Frontispiece(扉页论文)高亮推荐。本研究发现mRNA ac4C修饰通过NAT10/SEPT9/HIF-1a正反馈回路,导致HIF-1通路过度激活,诱导糖酵解成瘾,提高胃癌细胞缺氧耐受性;还发现mRNA ac4C修饰与抗血管生成治疗抵抗之间的相关性,揭示了mRNA ac4C修饰调控细胞缺氧耐受性的新机制,并提出了通过apatinib联合ac4C抑制剂以克服抗血管生成治疗抵抗的潜在治疗策略。表观生物为此研究提供了acRIP-seq、Ribo-seq以及mRNA-seq技术服务。

研究者通过人体胃癌组织及抗血管生成治疗抵抗模型发现ac4C“writer”蛋白-乙酰转移酶NAT10于缺氧区域中高度富集。通过探索调控NAT10表达的上游关键因素,发现负责调控低氧稳态的关键转录因子HIF-1a通过结合NAT10启动子上的缺氧反应元件调控其转录,促进NAT10在缺氧微环境中的动态上调。
然而,研究人员通过RNA-seq以及功能验证发现,乙酰转移酶NAT10可能反向调控HIF-1通路。NAT10可能通过激活HIF-1通路,促进己糖激酶(HK)、丙酮酸脱氢酶激酶(PDK)等关键酶的转录促进胃癌细胞葡萄糖代谢重编程。这提示NAT10与HIF-1a之间可能存在反馈回路。为了阐明NAT10调控胃癌细胞缺氧耐受性的具体机制,研究人员进行acRIP-seq与Ribo-seq测序分析(表观生物提供)。经acRIP-seq测序分析发现mRNA ac4C peak呈现为经典的CXXCXX特征结构,并主要分布于mRNA的CDS上(图1A-1D)。
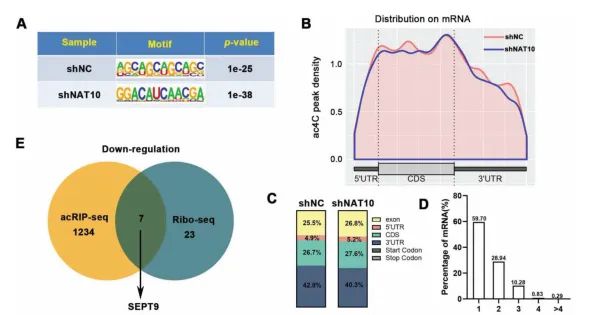
图1 胃癌细胞mRNA ac4C修饰特点
经acRIP-seq及Ribo-seq联合分析筛选(图1E),发现NAT10介导的ac4C修饰显著提高SEPT9 mRNA的翻译效率与稳定性,同时通过双荧光素酶报告实验证实调控SEPT9 mRNA稳定性的关键ac4C修饰位点位于3'UTR上。
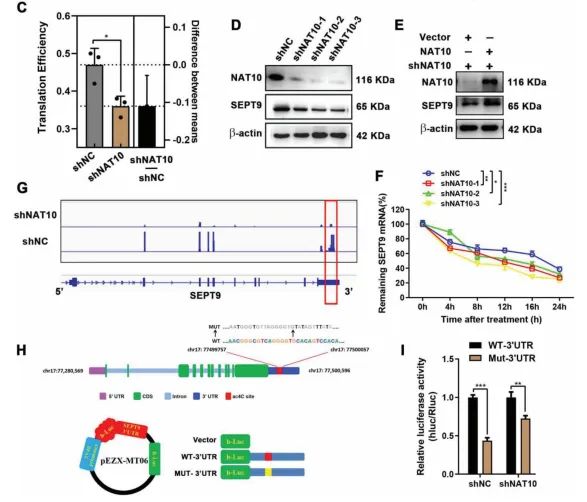
图2 ac4C修饰提高SEPT9 mRNA翻译效率及稳定性(acRIP-seq与 Ribo-seq测序及联合分析服务由表观生物提供)
此外,研究人员进一步发现在胃癌细胞中SEPT9作为载体促进HIF-1a的转移入核。因此形成了NAT10/SEPT9/HIF-1a的正反馈回路,持续激活HIF-1通路,导致HK、PDK表达上调,引导碳通量流向糖酵解,诱导糖酵解成瘾,使胃癌细胞耐受抗血管生成治疗抵抗所诱导的缺氧微环境。基于以上发现,研究人员提出了抗血管生成(apatinib)与ac4C抑制剂(Remodelin)协同互补的联合治疗策略。减少肿瘤血供的同时阻断葡萄糖代谢重编程,克服抗血管生成治疗抵抗,增强抗肿瘤效应,为改进胃癌治疗提供新思路。
作者介绍
南方医科大学南方医院李国新教授、叶耿泰副研究员及李风萍医师为论文共同通讯作者,南方医科大学南方医院杨庆斌博士后、雷雪涛博士、何嘉勇博士、彭燕梅博士为论文共同第一作者。该项研究工作得到了国家自然科学基金、中国博士后科学基金和广东省胃肠肿瘤精准微创诊疗重点实验室等项目的资助。
原文:Yang Q, Lei X, He J, et al. N4-Acetylcytidine Drives Glycolysis Addiction in Gastric Cancer via NAT10/SEPT9/HIF-1α Positive Feedback Loop. Adv Sci (Weinh). 2023 Jun 16:e2300898.
m6A、m1A、m7G、ac4C、m6Am、假尿嘧啶修饰测序服务
表观生物拥有多种RNA修饰测序服务,包括meRIP-seq(点击了解)、acRIP-seq(点击了解)、m1A-seq、TRAC-seq(点击了解)、PA-ψ-seq(点击了解)、m6Am-seq、ONT Direct RNA全长转录组测技术(点击了解)等,为研究者绘制全转录组RNA修饰图谱;表观生物还提供SELECT检测试剂盒(点击了解),填补市场上特定位点m6A常规检测技术的空白,可应用于鉴定m6A相关蛋白的作用靶点,深入挖掘m6A修饰的作用机制!以上技术与我司Ribo-seq、SLAM-seq技术结合,构建完备的RNA修饰研究解决方案;还可与ChIP-seq、HiChIP等表观基因组学进行创新组合,打破组学壁垒,冲刺高分文章!
表观生物提供表观组学测序研究解决方案

表观生物完备的m6A修饰研究解决方案



